Původ a vlastnosti vody: Zázrak z hlubokého vesmíru, který nám teče z kohoutku

Rozhodl jsem se proto zpracovat toto téma pěkně do hloubky a připravil jsem pro vás třídílnou sérii. Dnes, v prvním díle, vás vezmu na úplný začátek. Podíváme se na to, kde se ta průhledná tekutina vzala, proč pijeme něco, co je starší než naše vlastní sluneční soustava, a jak jeden chemický "Mickey Mouse" drží náš svět pohromadě.
Původ vody ve vesmíru: Mezihvězdný koktejl starší než naše Slunce
Kde se tu všechna ta voda vlastně vzala? Ve škole se často učíme, že nám ji na Zemi přinesly bombardující komety a asteroidy v době, kdy naše planeta byla jen nehostinnou žhavou koulí. A to je z velké části pravda. Jenže příběh téhle kapaliny začíná ještě mnohem dál v minulosti.
Většina molekul H2O, které teď máte ve své sklenici, nevznikla tady. Zformovaly se v mrazivém, temném prachoplynném mračnu miliony let předtím, než se vůbec zažehla termonukleární fúze v našem Slunci. Atomy vodíku (vůbec nejstaršího a nejběžnějšího prvku, který vznikl hned po Velkém třesku) se v tomto prastarém mračnu potkaly s atomy kyslíku.
Kde se ale v prázdném vesmíru vzal kyslík? Aby mohl vzniknout, vesmír potřeboval gigantické termonukleární reaktory – hvězdy starších generací. Tyto první obří hvězdy ve svých žhavých jádrech obrovským tlakem doslova "upekly" z lehkých prvků ty těžší, včetně kyslíku. Když pak tyto stárnoucí hvězdy na konci svého života explodovaly jako supernovy, rozmetaly tuto cennou kyslíkovou úrodu do temnoty. Tam se kyslík potkal s všudypřítomným vodíkem. Kdykoliv se tedy napijete, dáváte si vlastně prastarý mezihvězdný koktejl, za který zaplatily životem hvězdné generace před námi.

(Ilustrace: Chemický Mickey Mouse)
Infobox:
Věděli jste, že voda ve vesmíru překvapivě není vůbec vzácná? Najdeme ji v kometách a mezihvězdných objektech, tvoří velkou část prstenců planety Saturn a najdeme ji i na měsících vzdálených planet, jako je Europa nebo Enceladus. Háček je v tom, že je tam buď v podobě tvrdého ledu, nebo řídkého plynu.Kapalná voda na Zemi: Proč je modrá planeta tak neuvěřitelně vzácná
To, co dělá naši Zemi tak astronomicky výjimečnou, tedy není samotná přítomnost molekul H2O. Vody je všude plno. To, co je vzácnější než zlato, je fakt, že tu máme ideální podmínky pro to, aby se voda udržela v kapalném skupenství. A navíc přímo na povrchu!
Země se nachází v takzvané obyvatelné zóně – nejsme ani moc blízko Slunci, aby se nám oceány vyvařily do vesmíru, ani příliš daleko, abychom zamrzli na kost. Máme navíc dostatečnou gravitaci a hustou atmosféru, která vytváří potřebný tlak. Zatímco zlato a těžké kovy běžně vznikají při srážkách neutronových hvězd a po vesmíru jich poletuje obrovské množství, obrovské oceány kapalné vody pod širým (a dýchatelným) nebem jsme zatím nikde jinde s jistotou nepotvrdili.
Infobox:
Jak se "vyrábí" voda? Smíchat plyny nestačí!Možná vás napadne: Když víme, že voda je H2O, proč prostě nesmícháme vodík a kyslík v továrně a nevyřešíme tak sucho na planetě? Má to jeden ohlušující háček.
Když dáte tyto dva plyny do jedné místnosti, nestane se vůbec nic. Molekuly plynného vodíku (H2) i kyslíku (O2) jsou samy o sobě spárované a spokojené. Ignorují se. Abyste je donutili se rozpojit a vytvořit novou sloučeninu (H2O), musíte jim dodat aktivační energii.
Stačí jediná jiskra. Ta roztrhá původní vazby a atomy se na sebe okamžitě a agresivně vrhnou, protože molekula vody je energeticky mnohem stabilnější. A jak velí fyzika – při přechodu do stabilnějšího stavu se obrovské množství přebytečné energie uvolní do okolí.
Spojení vodíku a kyslíku je tak jednou z nejvýbušnějších reakcí v přírodě (což se stalo osudným i vzducholodi Hindenburg). Právě proto tuto reakci nepoužíváme k výrobě pitné vody, ale k letům do kosmu! Obří centrální stupeň rakety SLS, která vynáší misi Artemis k Měsíci, nedělá nic jiného, než že řízeně míchá a zapaluje tekutý vodík s kyslíkem. Ten neuvěřitelný oheň a oblaka "kouře", které raketu zvedají, je ve skutečnosti jen brutálně žhavá vodní pára.
Molekula H2O a polarita: Chemický Mickey Mouse jako dokonalý magnet
Proč je ale zrovna voda tak kriticky důležitá pro vznik života? Tajemství se skrývá v tom, jak je samotná molekula postavená a jak fungují její chemické vazby. Molekula vody (jeden velký atom kyslíku a dva malé atomy vodíku) totiž není poskládaná rovně jako nějaká činka. Vypadá přesně jako hlava Mickey Mouse. Kyslík je hlava a vodíky tvoří uši, které trčí do jedné strany.
Tenhle zdánlivě banální, asymetrický tvar způsobuje naprostou fyzikální magii. "Hlava" (kyslík) si k sobě stahuje elektrony silněji, takže má lehký záporný náboj, zatímco "uši" (vodíky) mají náboj kladný. Voda je tedy takzvaně polární molekula – funguje jako malinký magnet s plusem a mínusem.
A právě to z ní dělá nejbrutálnější rozpouštědlo na planetě. Představte si, že do hrnce s vodou hodíte zrnko soli (chlorid sodný). Zrnko soli není tvořeno izolovanými molekulami, je to pevná 3D mřížka, kde se střídá kladný sodík a záporný chlor. Jakmile toto zrnko spadne do vody, mikromagnety H2O zafungují jako demoliční četa. Záporné "hlavy" kyslíku obklíčí sodík, zatímco kladné "uši" vodíku se nalepí na chlor.
Voda tuto pevnou solnou mřížku doslova rozebere na jednotlivé atomy (ionty) a každý z nich uzavře do malé vodní bubliny, aby se nemohly spojit zpátky. Sůl tedy z vody nezmizela, nevypařila se, ani se neproměnila ve vodu. Jen její rozložené, poletující ionty tak dokonale splynuly s vodním davem, že je okem nevidíme. Náš jazyk ale tyto plovoucí ionty sodíku a chloru okamžitě zaznamená – a to je ta slaná chuť, kterou cítíme. Bez této schopnosti rozpouštět a transportovat živiny by na Zemi nemohla fungovat vůbec žádná buňka.
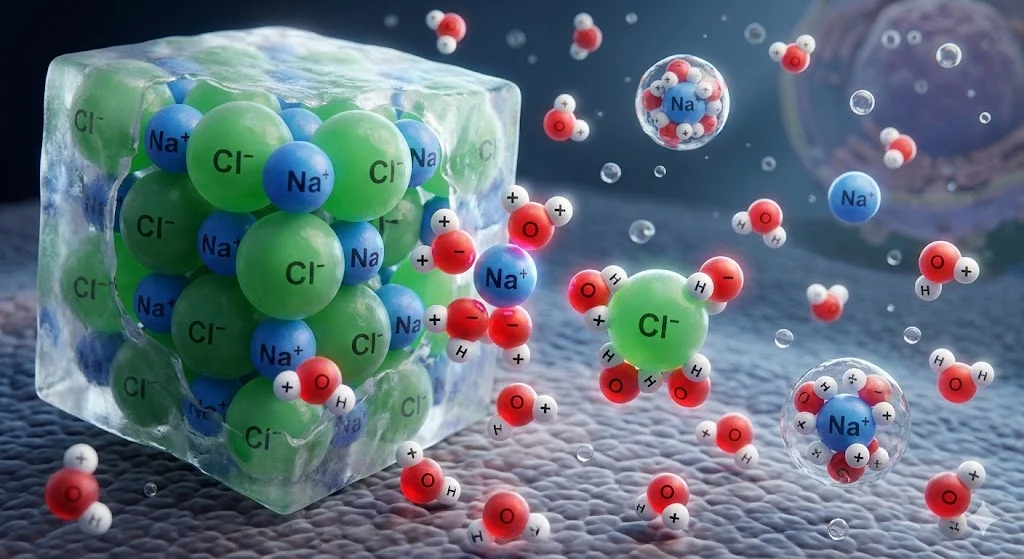
(Poznámka: Ilustrace je uměleckou vizualizací. Ve skutečnosti ionty nejsou zalité v žádné 'kostce ledu' a netvoří kolem sebe fyzické bubliny, ale molekuly vody je volně obklopují.)
Vodíkové můstky: Neviditelné ruce a tajemství povrchového napětí
Protože jsou molekuly vody jako malé magnety, přitahují se i samy k sobě. "Ouškem" jedné molekuly se přilepí k "hlavě" molekuly druhé. Vznikají takzvané vodíkové můstky. Já si to vždycky představuji, jako když se dav lidí chytne za ruce.
Tato neviditelná síť je neuvěřitelně pevná a způsobuje jev zvaný povrchové napětí. Určitě jste už někdy viděli bruslařku – malý hmyz, který klouže po hladině rybníka a nepotopí se. Bruslařka není magická, jen využívá toho, že se molekuly vody na hladině drží za ruce tak pevně, že vytvoří jakousi neviditelnou trampolínu, která lehký hmyz udrží. Díky stejnému principu dokáže voda "šplhat" mikroskopickými trubičkami v kmenech stromů až do stometrové výšky, a to zcela bez jakékoliv pumpy.
Fyzikální anomálie vody: Rebel, díky kterému nezmrzly oceány
Na závěr našeho prvního ponoru do mikrosvěta vody si musíme ukázat její největší rebélii proti fyzikálním pravidlům. Téměř všechny látky ve vesmíru se chovají stejně: když je zahřejete, roztáhnou se (jsou řidší), a když je ochladíte, smrsknou se (zhoustnou a ztěžknou). Zkuste si představit, že byste měli vanu plnou roztaveného železa a hodili do ní kostku pevného, zmrzlého železa. Okamžitě by klesla ke dnu.
Ale voda? Ta to má jinak. Když voda mrzne a mění se v led, její molekuly se uspořádají do krystalické mřížky, která mezi nimi paradoxně vytvoří více prázdného prostoru. Led je tedy o zhruba 10 % řidší a lehčí než kapalná voda. Proto kostky ledu ve vašem drinku plavou na hladině.
Zdá se to jako detail, ale pro Zemi to znamená hranici mezi životem a smrtí. Kdyby se led potápěl ke dnu jako normální slušně vychované látky, každou zimu by jezera a oceány začaly mrznout odspodu. Nakonec by zamrzly celé, od dna až po hladinu, a sluneční paprsky by je nikdy nedokázaly celé rozmrazit. Naše planeta by byla jen jedna velká, mrtvá ledová koule. Díky této anomálii ale led vytvoří na hladině izolační krustu a pod ním může vesele pokračovat život.

(Fyzikální anomálie vody: Rebel, díky kterému nezmrzly oceány)
Závěr a co nás čeká příště
Zatímco dnes jsme se pohybovali v mikroskopickém světě atomů a molekul, v příštím díle to vezmeme ve velkém. Podíváme se na to, jak tato ohromná masa vody na Zemi cestuje. Ukážeme si, jak funguje největší destilační přístroj na světě, co se ukrývá v obrovských podzemních nádržích a jak jsme se jako lidstvo naučili tento mocný živel spoutat, filtrovat i, bohužel, trochu poškodit.
Děkuji vám, že jste článek dočetli až do konce. Pokud se vám můj přístup k vědě, vesmíru a kritickému myšlení líbí, zvažte prosím vstup do Klubu zvědavců níže. Přes e-mail spolu můžeme zůstat v přímém kontaktu zcela nezávisle na tom, co zrovna dělají algoritmy sociálních sítí nebo vyhledávačů.