Periodická tabulka prvků a vznik hmoty: Jak hvězdy stvořily vše, co známe

Původ chemických prvků: Od Velkého třesku po výbuchy supernov
Představte si, že máte postavit fungující svět, ale na začátku dostanete k dispozici jen dva nejprostší stavební prvky. Přesně v takové situaci se nacházel náš vesmír krátce po svém vzniku. Po Velkém třesku existoval v podstatě jen vodík (nejjednodušší prvek) a helium. Vesmír byl chemicky sterilní. Nebyl tu uhlík pro život, kyslík pro dýchání, křemík pro skály ani železo pro krev.
Aby vznikla komplexní hmota, musel vesmír nastartovat obrovské tavící kotle – hvězdy. Uvnitř hvězd, jako je naše Slunce, panují tak extrémní podmínky, že dochází k jaderné fúzi. Hvězda funguje jako továrna, která drtí jednoduché atomy vodíku o sebe takovou silou, až se spojí v nové, těžší prvky.
Fascinující fakt: Všechny těžší prvky, jako je zlato ve vašem prstenu nebo vápník ve vašich kostech, vznikly při těch nejextrémnějších vesmírných srážkách – při výbuších supernov a kolizích vyhaslých neutronových hvězd. Jsme doslova stvořeni z hvězdného popela.
Mendělejevova tabulka: Co je atomová hmotnost a jak vnesla řád do chaosu
V 19. století chemie připomínala skladiště náhradních dílů bez katalogu. Vědci znali zlato, olovo či síru, ale netušili, jaký v tom je řád. Do tohoto chaosu vnesl světlo Dmitrij Ivanovič Mendělejev. Rozhodl se prvky seřadit, ale potřeboval klíč. Tím klíčem se stala atomová hmotnost.
Co to přesně znamená? Jak jsme si popsali v článku o vnitřním vesmíru a atomech, představte si atom jako malý batůžek. Uvnitř batohu (v jádře) jsou těžké kuličky – protony a neutrony. Čím více jich tam je, tím je batoh těžší.
- Vodík má v batohu jen 1 proton. Je nejlehčí.
- Uhlík jich má 12 (6 protonů + 6 neutronů).
- Zlato je extrémně těžké – nese jich 197.
Mendělejev v roce 1869 nemohl atomy vidět, ale uměl změřit, o kolik je daný plyn těžší než vodík. Když si tyto „váhy“ napsal na kartičky a seřadil je, všiml si fascinující pravidelnosti. Vlastnosti prvků se periodicky opakovaly. Lithium reagovalo stejně divoce jako Sodík. Mendělejev objevil, že hmota má svůj rytmus.
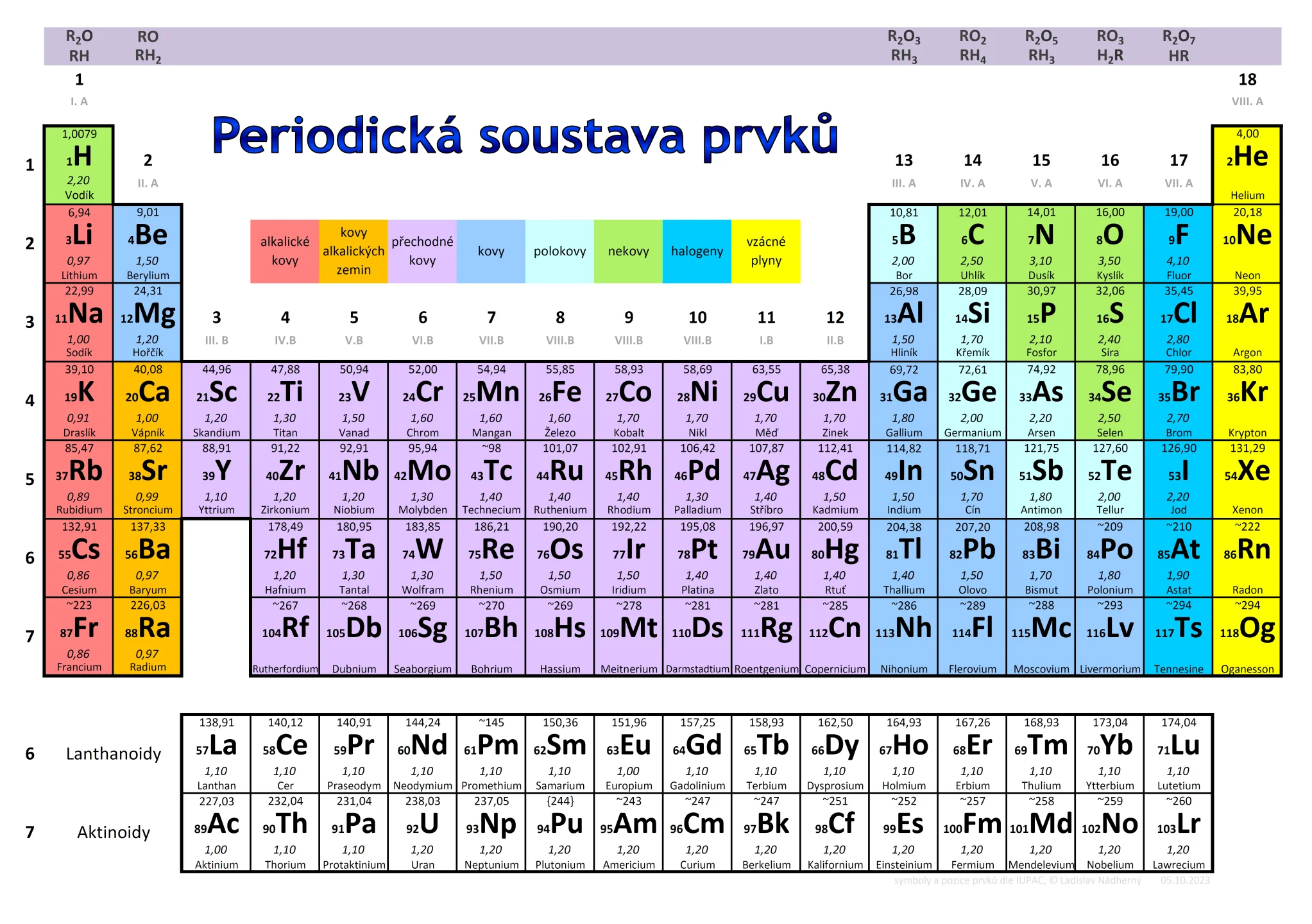
(Periodická tabulka prvků)
Infobox:
Jak číst v mapě hmoty? (Rodiny prvků)
Tabulka není jen seznam, je to geniálně seřazená mapa. Prvky, které bydlí ve stejném svislém sloupci (skupině), jsou jako příbuzní – mají podobnou povahu.
- Šlechtici (Vzácné plyny): Úplně vpravo bydlí prvky jako Helium nebo Neon. Říkáme jim „vzácné“, protože jsou to chemičtí snobi. S nikým se nebaví, s nikým nereagují. Jsou dokonalí a spokojení sami se sebou.
- Výbušní cholerici (Alkalické kovy): Úplně vlevo (kromě vodíku) bydlí Sodík nebo Draslík. Jsou to měkké kovy, které jsou zoufale nespokojené. Touží po reakci tak moc, že když je hodíte do vody, začnou hořet nebo vybuchnou.
- Životodárný střed: Mezi nimi najdeme Uhlík, Kyslík nebo Dusík – prvky, které nejsou tak nudné jako šlechtici, ani tak šílené jako cholerici. Jsou to mistři spolupráce, kteří tvoří základ života.
Mendělejev pochopil, že pokud má v tabulce pod sebou dva „choleriky“, musí pod ně patřit další cholerik, i když ho ještě nikdo neviděl.
Síla vědecké metody: Jak Mendělejev předpověděl neobjevené prvky
Tento moment je pro vědu klíčový a je dokonalou ukázkou vědecké metody v praxi. Když Mendělejev tabulku tvořil, narazil na problém. Aby mu jeho systém „period“ fungoval, musel na několika místech nechat prázdná místa. Prvky, které by tam měly pasovat, prostě nikdo neznal. Kritici se mu smáli: „Nemůžete stavět systém na něčem, co neexistuje.“
Mendělejev ale věřil logice svého systému. Prohlásil: „Ty prvky existují. Jen jsme je ještě neobjevili. A až je najdeme, budou mít přesně tyto vlastnosti.“ Například pod hliníkem nechal díru pro prvek „eka-aluminium“. O několik let později bylo objeveno Gallium. Jeho vlastnosti přesně odpovídaly Mendělejevově předpovědi. Dokázal popsat hmotu, kterou nikdy neviděl, pouze na základě pochopení řádu.

(Dmitrij Ivanovič Mendělejev)
Chemické vazby a vznik molekul: Proč a jak se atomy spojují?
Mít 92 druhů dílků je úžasné, ale ta pravá rozmanitost vzniká až jejich kombinací. Jak se ale atomy spojují? Nemají lepidlo ani šroubky. Mají elektrony.
Představte si atom jako sluneční soustavu. Uprostřed je těžké jádro a daleko kolem něj obíhají lehké elektrony. Ty fungují jako „ruce“, kterými se atomy dotýkají okolí. Každý atom touží po jediném – mít svou vnější vrstvu elektronů kompletně zaplněnou. Aby toho dosáhl, musí se spojit s někým jiným:
- Loupež (Iontová vazba): Agresivní atom (třeba Chlor) ukradne elektron jinému (Sodíku). Tím se z nich stanou opačně nabité magnety a pevně se k sobě přicvaknou. Tak vzniká sůl.
- Sdílení (Kovalentní vazba): Atomy se dohodnou, že budou elektrony sdílet, jako by se drželi za ruce. Takto se drží vodík a kyslík ve vodě.
Stačí prvky jen smíchat?
Možná vás napadne: Když dám dva prvky k sobě, vznikne hned molekula? Většinou ne – a to je naše štěstí! Kdyby to tak fungovalo, vzduch kolem nás by se okamžitě vznítil. Atomy si totiž chrání svůj „osobní prostor“ (odpuzují se svými obaly). Aby bariéru prolomily a chytily se za ruce, potřebují obvykle „pošťouchnout“ energií – teplem, tlakem nebo jiskrou. Teprve pak začne ta pravá chemická reakce.
Právě po těchto spojeních pátráme ve vesmíru. Když teleskopy hledají druhou Zemi, nehledají atomy, ale molekuly – chemické podpisy života.

(Dynamická scéna zobrazující iontovou vazbu jako krádež elektronu, kovalentní vazbu jako sdílení elektronů a energii potřebnou pro chemickou reakci.)
Transurany a Ostrov stability: Je seznam prvků konečný?
Možná vás napadla provokativní otázka: „Proč končíme číslem 92? Můžeme najít dílek číslo 93, 100 nebo 150?“ Odpověď zní ano i ne. Příroda je v tomto ohledu poměrně přísná, ale lidská zvědavost hranice neuznává.
V běžné přírodě je posledním a nejtěžším prvkem Uran (číslo 92). Cokoliv těžšího je pro vesmír příliš nestabilní. Představte si atomové jádro jako pytel plný naštvaných koček (kladných protonů). Ty se navzájem silně odpuzují. Silná jaderná síla (lepidlo) je sice drží pohromadě, ale u čísla 92 už je těch „koček“ tolik, že se pytel začíná trhat.

(AI ilustrace atomu Uranu)
Vědci v laboratořích (jako je CERN) však dokázali přírodu obejít. Ve srážkách částic uměle „nacpali“ do jader více protonů a vytvořili tak nové prvky – Neptunium (93), Plutonium (94) až po současného rekordmana Oganesson (118).
Problém je čas. Tyto supertěžké prvky jsou tak nestabilní, že se rozpadnou za zlomky sekundy. Často zmizí dřív, než je stihneme pořádně změřit. Znamená to konec tabulky?
Fyzikové věří, že ne. Teorie předpovídají existenci bájného „Ostrova stability“. Pokud bychom dokázali vyrobit prvek s „magickým číslem“ protonů (například 120 nebo 126) a správným počtem neutronů, vnitřní síly v jádře by se mohly znovu vyrovnat. Takový supertěžký prvek by se nerozpadl hned, ale mohl by vydržet minuty, dny nebo i roky. Byl by to zcela nový materiál s vlastnostmi, které si dnes neumíme ani představit.
Spektroskopie a 3I/Atlas: Jak na dálku zjišťujeme chemické složení vesmíru
Možná si říkáte, proč to řešíme na webu o vesmíru? Protože chemie je naším hlavním nástrojem při pátrání po mimozemském životě a původu těles.
Když naším systémem proletí záhadný objekt, jako je 3I/Atlas (o které jsme psali v souvislosti s potvrzením úniku vody), nemůžeme na ni přistát. Můžeme ale namířit teleskopy a pomocí spektroskopie „číst“ její chemické složení.

(Ilustrace: Interstelární kometa s neobvyklým chemickým složením je pozorována obřím pozemským teleskopem.)
Děkuji vám, že jste článek dočetli až do konce. Pokud se vám můj přístup k vědě, vesmíru a kritickému myšlení líbí, zvažte prosím vstup do Klubu zvědavců níže. Přes e-mail spolu můžeme zůstat v přímém kontaktu zcela nezávisle na tom, co zrovna dělají algoritmy sociálních sítí nebo vyhledávačů.